התגובה של האינטראקציה של CaCl2, H2SO4
אחד המכשולים במדרגות הראשונותהמחקר של סביבות כימיות יסודות הוא כתיבת תגובות כימיות. לכן, שאלות על האינטראקציה של CaCl2, H2SO4 הם אפילו לא מעת לעת, אבל באופן שיטתי. בואו ננתח את הרגעים העיקריים של "הבעיה".
שיא המשוואה המולקולרית
האינטראקציה בין סידן כלורי (מלח) וחומצה גופרתית מתמשכת בהתאם למנגנון החליפין.

- שני תרכובות בפתח (חומרים מתחילים);
- שני חיבורים לשקע (מוצרים);
- היעדר מוחלט של חומרים פשוטים.
על ידי החלפת קבוצות תגובה אחד עם השני, ריאגנטים הם השתנו, ואת המשוואה לוקח את הטופס:
CaCl2 + H2SO4 = CaSO4 + 2HCl.
כפי שניתן לראות, שני חומרים מורכבים, יונים המשתנים, יוצרים תרכובות שונות לחלוטין: מלח חדש (CaSO4) וחומצה הידרוכלורית (HCl).
אפשרות לזרום עד הסוף
אתה יכול בקלות לענות על שאלה זו על ידי כתיבת משוואת התגובה בצורה מולקולרית עבור CaCl2, H2SO4. מתוך סוג של מוצרים והכל יהיה תלוי. עד סוף התהליך הוא בתחום החינוך:
- חומר מסיס במקצת (משקע);
- תרכובת נדיפה (גז);
- מגיב נמוך ממיסים (מים, אלקטרוליט חלש).
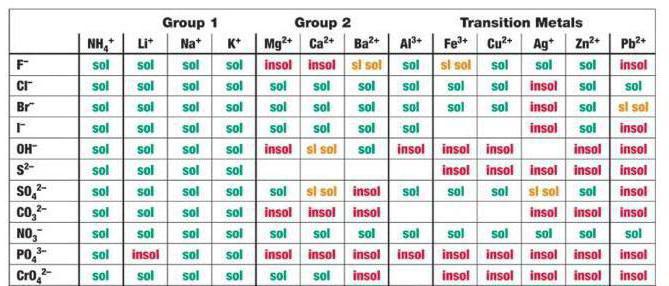
במקרה נחשב עבור CaCl2, H2SO4, בין מוצרי התגובה יש סולפט סידן, מתחם מסיס במשורה זירז על פי הטבלה.
כתוצאה מכך, תהליך החליפין יגיע עד הסוף.
הצורה היונית מופחתת של ההקלטה בין CaCl2, H2SO4
לאחר שציירנו את כל התרכובות מסיסות על יונים והפחתת קבוצות תגובה חוזרות, אנו מקבלים את שתי המשוואות הנדרשות:
- הצורה היונית הכוללת של ההקלטה בין CaCl2, H2SO4
ca2+ + 2cl- + 2h+ map map42- = caso4 + 2h+ + 2cl-
- צורה מופחתת של משוואה
ca2+ map map42- = caso4.
יש לזכור כי היונים צבועים רקמסיסים מסיסים, חומצות, בסיסים (זה נקבע בקלות על ידי שולחנות מיוחדים). אלקטרוליטים חלשים כגון פחם או חומצה אצטית כתובים תמיד בצורת מולקולרית.
עכשיו אתה יודע איך אינטראקציה בין סידן כלורי (מלח) וחומצה גופרתית מתרחש.

