שינויים Allotropic של חמצן: מאפיין השוואתי וערך
אטומים מסוג אחד יכולים להיות שוניםחומרים. עבור אלמנט המיועד על ידי הסמל "O" (מן השם הלטיני Oxygenium), שני חומרים פשוטים נפוצים ידועים בטבע. הנוסחה של אחד מהם היא O2, השני - O3. אלה שינויים allotropic של חמצן (allotropes). ישנם תרכובות אחרות שהן יציבות פחות (O4 ו O8). כדי להבין את ההבדל בין צורות אלה יעזור להשוות מולקולות ומאפיינים של חומרים.
מהם שינויים allotropic?
אלמנטים כימיים רבים יכולים להתקייםשניים, שלושה או יותר. כל אחד משינויים אלה נוצר על ידי אטומים מאותו המין. המדען י 'ברזליוס בשנת 1841 היה הראשון שקרא לתופעה כזאת אלוטרופיה. הסדירות הפתוחה שימשה במקור רק כדי לאפיין את החומרים של המבנה המולקולרי. לדוגמה, שני שינויים allotropic של חמצן ידועים, האטומים מהם יוצרים מולקולות. מאוחר יותר, החוקרים קובעים כי השינויים עשויים להיות בין הגבישים. על פי המושגים המודרניים, allotropy הוא אחד המקרים של פולימורפיזם. ההבדלים בין צורות נגרמים על ידי מנגנונים של היווצרות של קשר כימי במולקולות ובגבישים. תכונה זו מתבטאת בעיקר באלמנטים של קבוצות 13-16 של הטבלה המחזורית.

כיצד שילוב אחר של אטומים משפיע על תכונות החומר?
שינויים Allotropic של חמצן ואוזוןהם נוצרו על ידי האטומים של אלמנט עם מספר מס '8 ומספר זהה של אלקטרונים. אבל הם שונים במבנה, אשר גרמה פער משמעותי המאפיינים.
| תסמינים | חמצן | אוזון |
הרכב המולקולה | 2 אטומי חמצן | 3 אטומי חמצן |
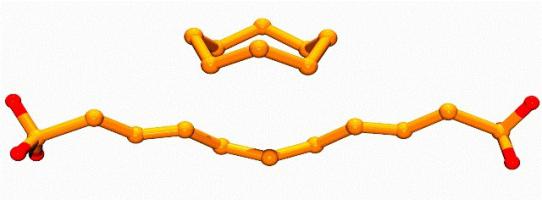
| מבנה |  | |
| מצב וצבע מצטברים | גז שקוף חסר צבע או נוזל כחול חיוור | גז כחול, נוזל כחול, סגול כהה מוצק |
| ריח | חסר | חדה, מזכירה רעם, חציר טרי |
נקודת התכה (° C) | -219 | -193 |
| נקודת רתיחה (° C) | -183 | -112 |
צפיפות (g / l) | 1,4 | 2,1 |
מסיסות במים | מעט מסיסים | טוב יותר מאשר חמצן |
פעילות כימית | בתנאים רגילים, יציב | קל להתפרק עם היווצרות של חמצן |
מסקנות מתוצאות ההשוואה: שינויים אלוטרופיים של חמצן אינם שונים בהרכב האיכותי. מבנה המולקולה משתקף בתכונות הפיסיקליות והכימיות של החומרים.
האם אותה כמות של חמצן ואוזון בטבע?
חומר אשר נוסחה O2, מתרחשת באטמוספרה, הידרוספרה, יבשתיקליפות ואורגניזמים חיים. כ -20% מהאוויר נוצר על ידי מולקולות חמצן דיאטומיות. בסטרטוספירה בגובה של כ 12-50 ק"מ מפני השטח של כדור הארץ יש שכבה בשם "מסך האוזון". הרכבו משקף את הנוסחה O3. אוזון מגן על הפלנטה שלנו על ידי ספיגתקרניים מסוכנות של הספקטרום האדום והאולטרה סגול של השמש. ריכוז החומר משתנה כל הזמן, וערכו הממוצע נמוך - 0.001%. לפיכך, O2 ו O3 - שינויים allotropic של חמצן, אשר יש הבדלים משמעותיים התפוצה שלהם בטבע.
כיצד לקבל חמצן ואוזון?

שינויים Allotropic של חמצן וגופרית
האלמנטים הכימיים O (Oxygenium) ו- S (גופרית)ממוקמים באותה קבוצה של הטבלה המחזורית, הם מאופיינים על ידי היווצרות של צורות allotropic. של מולקולות עם מספר שונה של אטומי גופרית (2, 4, 6, 8) בתנאים רגילים, היציב ביותר הוא S8, הדומה כתר בצורת. גופרית מעוין ומונוקליני הם בנויים ממולקולות 8-atom כאלה.

בקנה מידה תעשייתי,תכונות חמצון של צורות שונות. אוזון משמש לחיטוי של אוויר ומים. אבל בריכוז מעל 0.16 מ"ג למ"ק, הגז הזה מסוכן לבני אדם ולבעלי חיים. חמצן מולקולרי חיוני לנשימה, הוא משמש בתעשייה וברפואה. Allotropes של פחמן (יהלום, גרפיט), זרחן (לבן, אדום) ואלמנטים כימיים אחרים ממלאים תפקיד חשוב בפעילות הכלכלית.








